ここ最近、いわゆる "免疫細胞" 領域における先端研究の成果に関心を寄せ続けている。この領域でのアグレッシィブとも言える研究が、従来、"そのメカニズムが不明" 扱いとされてきたいろいろな難しい疾患に、あたかも光明をもたらすかのような可能性が覗えるようだから、大いに期待したいわけなのである。
"免疫(応答)" というと、生体内部で "自分(のからだ)" を "敵" から守ってくれる "自前の味方" 勢力だと受け止められがちだ。
◆ 参照 <免疫応答【メンエキオウトウ】――免疫を担当する細胞が外来性および内因性の異物を抗原と認識し、特異的に応答して行われる反応。>( kotobank.jp )
ただし、"手放し" で "100% の味方" とばかりは称賛できないという複雑さがある。
たとえば、"自己免疫疾患" と呼ばれている "花粉症アレルギー/リウマチ"( 臓器移植に伴う "拒絶反応" も )などがその例であり、"自分(のからだ)" に潜む "免疫細胞" 領域のメカニズム/働き自体が、"自分(のからだ)" を蝕み、苦痛や害をもたらすという "反転攻勢" に打って出ている......。
今回、注目する記事は、こうした、いわば "免疫細胞" の "ご乱心騒動(?) に対して "新たな一矢を報いる!" 研究成果だと言えそうだ。
この研究成果を伝えているのは、下記引用サイト記事 : 細胞死や免疫応答を調節する新たな分子メカニズムを発見/東京大学/2014.01.22 である。
先ず、当研究成果を理解し易いように、<研究の背景> を踏まえておきたい。
<生体内での活性酸素の過剰な産生は、生体を構成するタンパク質やDNA、細胞膜などに傷害を与え、修復できない程度まで細胞が障害を受けると細胞死が誘導されます。このような活性酸素で誘導される細胞死は、心筋梗塞や脳梗塞といった虚血性疾患や神経変性疾患、糖尿病、がんなどさまざまなヒトの疾患に関与することが知られています。また、過剰な免疫応答は、強いアレルギー反応や炎症を引き起こし、ぜんそくや皮膚炎、リウマチなどの自己免疫疾患につながります。しかしながら、このような細胞死や免疫応答が、どのような仕組みによって調節されているかについては、不明な点が残されていました>( 下記引用サイト記事 )
この<不明な点が残されていました> とある<仕組み> が解明されたわけだが、"免疫細胞" 領域での基礎知識がない丸腰ではいささか難しい。
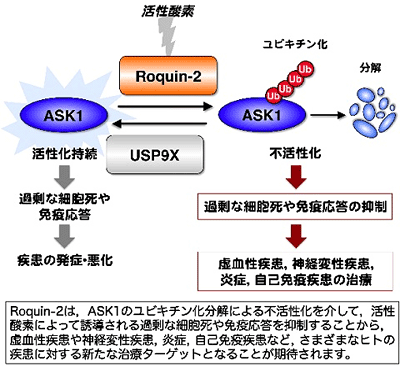
<東京大学大学院薬学系研究科の一條秀憲教授、松沢厚特任准教授、丸山剛元特任研究員らの研究グループは、これまでに活性酸素によって誘導される細胞死や免疫応答を促進する細胞内のシグナル伝達分子(注2)であるタンパク質ASK1を発見し研究を進めてきました。今回の研究では、ASK1の分解を促進させる新たなタンパク質Roquin-2を発見しました。Roquin-2は、分解されるべきタンパク質の目印となる分子、ユビキチン(注3)をASK1に結合することで、ASK1の分解を促進させ、不活性化させます。この仕組みにより、生体内で起こる過剰な細胞死や免疫応答が適切に調節されていることが示唆されました。
本成果により、ASK1の活性を調節するRoquin-2のようなタンパク質を標的とすることで、活性酸素誘導性の細胞死が関与する神経変性疾患や炎症、自己免疫疾患など、さまざまなヒトの疾患に対する新たな治療薬の開発につながると期待されます> とある。
ところで、この研究成果の一つのポイントは、<ASK1>という<シグナル伝達分子>であろうかと思われる。
実は、昨日の当誌の末尾で書いた<"情報伝達分子">のことなのである。
◆ 参照 <"免疫細胞" の範疇で重要な働きをしつつ、まだまだ未解明とされているさまざまな "情報伝達分子" の働きが解明される過程で、今後、さらに驚くべき未知の扉が開かれるのではないか>( "脳内免疫細胞"が自閉症や強迫性障害(OCD)で懸念される"社会的行動の形成"を助ける!( 当誌 2014.02.06 ) )
現在の"免疫細胞" 領域における先端研究の一つの焦点はこの辺に潜んでいるのかもしれない......。
細胞死や免疫応答を調節する新たな分子メカニズムを発見/東京大学/2014.01.22
東京大学大学院薬学系研究科1.発表者:
一條秀憲(東京大学大学院薬学系研究科 教授)
松沢厚(東京大学大学院薬学系研究科 特任准教授)
丸山剛(元 東京大学大学院薬学系研究科 特任研究員)2.発表のポイント:
◯ 神経変性疾患や糖尿病、アレルギー・炎症などで見られる過剰な細胞死や免疫応答を抑制するタンパク質(Roquin-2)を同定しました。
◯ タンパク質Roquin-2は、活性酸素により誘導される過剰な細胞死や免疫応答を促進するタンパク質を分解して抑制できることを見出しました。
◯ 本成果は、活性酸素によって誘導される細胞死が関与する、神経変性疾患や炎症などの疾患に対する新たな治療薬の開発に貢献するものと期待されます。3.発表概要:
活性酸素(注1)によって誘導される細胞死は、脳や心臟などの虚血性臓器障害やパーキンソン病といった神経変性疾患、糖尿病、がんなど、さまざまなヒトの疾患に関わります。また、過剰な免疫応答はアレルギーや炎症を引き起こし、ぜんそくやリウマチなどの自己免疫疾患につながります。しかし、このような細胞死や免疫応答がどのような分子機構で調節されているかについては、不明な点が残されていました。
東京大学大学院薬学系研究科の一條秀憲教授、松沢厚特任准教授、丸山剛元特任研究員らの研究グループは、これまでに活性酸素によって誘導される細胞死や免疫応答を促進する細胞内のシグナル伝達分子(注2)であるタンパク質ASK1を発見し研究を進めてきました。今回の研究では、ASK1の分解を促進させる新たなタンパク質Roquin-2を発見しました。Roquin-2は、分解されるべきタンパク質の目印となる分子、ユビキチン(注3)をASK1に結合することで、ASK1の分解を促進させ、不活性化させます。この仕組みにより、生体内で起こる過剰な細胞死や免疫応答が適切に調節されていることが示唆されました。
本成果により、ASK1の活性を調節するRoquin-2のようなタンパク質を標的とすることで、活性酸素誘導性の細胞死が関与する神経変性疾患や炎症、自己免疫疾患など、さまざまなヒトの疾患に対する新たな治療薬の開発につながると期待されます。
本成果は、2014年1月21日(米国時間)に、米国の科学雑誌「Science Signaling」のオンライン版に公開されます。なお、本研究は、文部科学省脳科学研究戦略推進プログラムの一環として、また科学研究費補助金、先駆的医薬品・医療機器研究発掘支援事業、ならびに最先端・次世代研究開発支援プログラムなどの助成を受けて行われました。―― 用語解説:
(注1) 活性酸素:スーパーオキシド、ヒドロキシラジカル、過酸化水素、一重項酸素など、酸素に由来する反応性の高い分子の総称。ミトコンドリアでのエネルギー産生や細胞膜での酵素反応等によって生成される。
(注2) シグナル伝達分子:細胞内外のさまざまな環境の変化を感知し、その情報を核や細胞内の小器官へと伝達する一連の分子群。
(注3) ユビキチン:76個のアミノ酸からなる比較的小さなタンパク質で、他のタンパク質の修飾に用いられ、タンパク質分解やDNA修復、小胞膜輸送、シグナル伝達など多様な生理機能に関わる。特にユビキチンが共有結合によって鎖状に連なったポリユビキチンは、タンパク質分解酵素複合体であるプロテアソームによって認識され、分解されるべきタンパク質の目印となることが分かっている。 ......―― 以下略 ――
8.添付資料:
( ※引用者注 ―― 文意を損なわないよう留意して割愛しています。)
<シグナル伝達分子>(<"情報伝達分子">)という、いわば"免疫細胞" 領域での "ネットワークにおける情報の働き!" への興味が尽きない...... (2014.02.07)







コメントする